Vesículas extracelulares
Las vesículas extracelulares (VE) incluyen una amplia gama de partículas de membrana lipídica secretadas por todos los tipos de células, distintas en tamaño, biogénesis, moléculas de carga y función. Después de ser segregadas mediante la fusión de cuerpos multivesiculares con la membrana plasmática, las VE desempeñan papeles centrales en una gran variedad de procesos, incluyendo comunicación intercelular, reciclaje de proteínas de membrana y lípidos, inmunomodulación, senescencia, angiogénesis, proliferación, diferenciación y migración. Curiosamente, se han encontrado VE en diferentes fluidos biológicos (por ejemplo, sangre, orina, saliva) y se consideran herramientas de diagnóstico relevantes y una fuente clave en la búsqueda de nuevos biomarcadores para enfermedades.
Por otro lado, las respuestas inmunes no deseadas han obstaculizado drásticamente los resultados después del trasplante alogénico de órganos y la terapia celular, y también conducen a todo tipo de enfermedades inflamatorias y relacionadas con autoinmunidad. Entre otros, las células madre mesenquimales tienen un poderoso potencial inmunomodulador, y sus VE están previstas como una fuente natural de nanopartículas capaces de aumentar los beneficios en el trasplante de órganos y controlar las enfermedades inflamatorias. De hecho, dado que las VE son aparentemente bien toleradas, su uso prepara el camino para innovadoras y más eficientes terapias libres de células que puedan evitar los efectos secundarios asociados al trasplante de células madre.
En términos de direcciones futuras, para lograr una translación clínica y una fabricación correcta, el desarrollo de terapias con vesículas extracelulares tiene que abordar hitos destacados como el procesamiento a gran escala en condiciones obligatorias de Buenas Prácticas de Fabricación, controles de calidad y potencia e instrumentación. En consecuencia, muchos factores en los procesos de aislamiento, caracterización y análisis pueden tener un impacto en el resultado de la producción de estas vesículas, pero también refinar en gran medida su extraordinaria eficacia. Aunque el diseño y desarrollo de productos basados en vesículas extracelulares està avanzando hacia procesos estandarizados y controlados a la escala adecuada, existen diferentes cultivos celulares o condiciones microambientales que pueden afectar en gran medida el rendimiento de las vesículas extracelulares y sus propiedades intrínsecas. Además, el uso de biorreactores con alta superficie para crecimiento celular, recirculación de medios de cultivo y recuperación continuada de vesículas es muy prometedora. Además, la implementación de ensayos rutinarios para evaluar la potencia y dosis óptimas son de suma importancia. Actualmente, sin técnicas robustas para su cuantificación, el control de possibles variaciones lote a lote es imprescindible. Por último, se debe invertir esfuerzos en el desarrollo de plataformas analíticas más con el objectivo de estudiar su carga molecular y predecir sus posibles beneficios o efectos secundarios tres su administración en pacientes. Con este fin, se deben lograr avances en las estrategias de purificación y análisis específicos mediante tecnologías omicas.
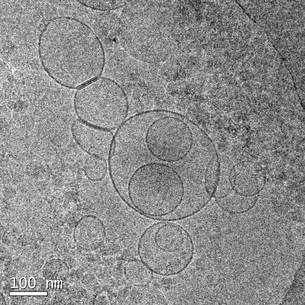
Vesículas extracelulares en una muestra de sangre periférica de donante sano
Recientemente, el grupo ha puesto a punto el desarrollo de un nuevo producto de terapia avanzada basado en la ingeniería de tejidos cardíaca. El nuevo producto contiene vesículas extracelulares derivadas de células madre mesenquimales de grasa cardiaca. Básicamente, el nuevo parche terapéutico, que puede adherirse directamente sobre la zona infartada mediante el uso de una cola quirúrgica de uso rutinario en clínica, está formado por una porción de matriz extracelular de pericardio (la membrana que rodea el corazón humano) que se ha descelularizado previamente y vuelta a rellenar posteriormente con las vesículas que tienen un tamaño de entre 50 y 150 nanómetros. El nuevo prototipo de terapia avanzada ha sido implantado con éxito en cerdos a los que se ha inducido un infarto agudo de miocardio. Los experimentos que se han llevado a cabo en el Centro de Medicina Comparada y Bioimagen ha permitido analizar el beneficio al cabo de una semana de la fijación del bioiumplante lleno de nanovesículas. En particular se ha estudiado la regulación de la respuesta inflamatoria por parte de las nanovesículas que podría revertir los efectos adversos provocados por el infarto. Como resultado se ha observado la liberación de una parte del contenido de nanovesículas desde el bioimplante cardíaco dentro de la zona infartada, la formación de nuevos vasos sanguíneos y una reducción del nivel de infiltración de células inmunes (macrófagos y linfocitos T) dentro del miocardio dañado.
Monguió-Tortajada M, Prat-Vidal1 C, Martínez-Falguera D, Teis A, Soler-Botija C, Courageux Y, Munizaga-Larroudé M, Moron-Font M, Bayes-Genis A, Borràs FE, Roura S, Gálvez-Montón C. Acellular cardiac scaffolds enriched with MSC-derived extracellular vesicles limit ventricular remodelling and exert local and systemic immunomodulation in a myocardial infarction porcine model. Theranostics 2022; 12(10):4656-4670.
Soler-Botija C, Monguió-Tortajada M, Munizaga-Larroudé M, Gálvez-Montón C, Bayes-Genis A, Roura S. Mechanisms governing the therapeutic effect of mesenchymal stromal cell-derived extracellular vesicles: A scoping review of preclinical evidence. Biomed Pharmacother. 2022 Mar;147:112683.
Courageux Y, Monguió-Tortajada M, Prat-Vidal C, Bayes-Genis A, Roura S. Clinical translation of mesenchymal stromal cell extracellular vesicles: Considerations on scientific rationale and production requisites. J Cell Mol Med. 2022 Feb;26(3):937-939.
Roura S, Monguió-Tortajada M, Prat-Vidal C, Gálvez-Montón C, Bayes-Genis A. Our Journey Through Advanced Therapies to Reduce Post-Infarct Scarring. Stem Cell Rev and Rep 2021 May 22.
Monguió-Tortajada M, Prat-Vidal C, Moron-Font M, Clos-Sansalvador M, Calle A, Gastelurrutia P, Cserkoova A, Morancho A, Ramírez MA, Rosell A, Bayes-Genis A, Gálvez-Montón C, Borràs FE, Roura S. Local administration of porcine immunomodulatory, chemotactic and angiogenic extracellular vesicles using engineered cardiac scaffolds for myocardial infarction, Bioactive Materials. 2021;6:3314-3327
Monguió-Tortajada M, Bayes-Genis A, Rosell A, Roura S.. Are mesenchymal stem cells and derived extracellular vesicles valuable to halt the COVID-19 inflammatory cascade? Current evidence and future perspectives.. Thorax. 2020 Dec 15;76(2):196-200. doi: 10.1136/thoraxjnl-2020-215717
Roura S, Monguió-Tortajada M, Munizaga-Larroudé M, Clos-Sansalvador M, Franquesa M, Rosell A, Borràs FE. Potential of Extracellular Vesicle-Associated TSG-6 from Adipose Mesenchymal Stromal Cells in Traumatic Brain Injury. Int J Mol Sci. 2020 Sep 15;21(18):6761. doi: 10.3390/ijms21186761
Andrés Miguez, Sara Fernández-García, Marta Monguió-Tortajada, Georgina Bombau, Mireia Galofré, María García-Bravo, Cristina Vila, Phil Sanders, Santiago Roura, Jordi Alberch, José Carlos Segovia, Nicholas D. Allen, Francesc E. Borràs, Josep M. Canals. In vivo progressive degeneration of Huntington’s disease patient-derived neurons reveals human-specific pathological phenotypes. BioRxiv. 2020. Doi: https://doi.org/10.1101/2020.10.21.347062
Cabrera-Pérez R, Monguió-Tortajada M, Gámez-Valero A, Rojas-Márquez R, Borràs FE, Roura S, Vives J. Osteogenic commitment of Wharton's jelly mesenchymal stromal cells: mechanisms and implications for bioprocess development and clinical application. Stem Cell Res Ther. 2019 Nov 28;10(1):356. doi: 10.1186/s13287-019-1450-3
Roura S, Monguió-Tortajada M, Borràs FE. Technical challenges for extracellular vesicle research towards clinical translation. Eur Heart J. 2019 Oct 3
Monguió-Tortajada M, Gálvez-Montón C, Bayes-Genis A, Roura S, Borràs FE. Extracellular vesicle isolation methods: rising impact of size-exclusion chromatography. Cell Mol Life Sci. 2019 Mar 19
Roura S, Vives J. Extracellular vesicles: Squeezing every drop of regenerative potential of umbilical cord blood. Metabolism. 2019 Jun;95:102-104
Roura S, Bayes-Genis A. Toward Standardization of Mesenchymal Stromal Cell-Derived Extracellular Vesicles for Therapeutic Use: A Call for Action. Proteomics. 2019 Jan;19(1-2):e1800397
Roura S, Gámez-Valero A, Lupón J, Gálvez-Montón C, Borràs FE, Bayes-Genis A. Proteomic signature of circulating extracellular vesicles in dilated cardiomyopathy. Lab Invest. 2018 Oct;98(10):1291-1299
Roura S, Gálvez-Montón C, de Gonzalo-Calvo D, Valero AG, Gastelurrutia P, Revuelta-López E, Prat-Vidal C, Soler-Botija C, Llucià-Valldeperas A, Perea-Gil I, Iborra-Egea O, Borràs FE, Lupón J, Llorente-Cortés V, Bayes-Genis A. Extracellular vesicles do not contribute to higher circulating levels of soluble LRP1 in idiopathic dilated cardiomyopathy. J Cell Mol Med. 2017 Nov;21(11):3000-3009
Monguió-Tortajada M, Roura S, Gálvez-Montón C, Pujal JM, Aran G, Sanjurjo L, Franquesa M, Sarrias MR, Bayes-Genis A, Borràs FE. Nanosized UCMSC-derived extracellular vesicles but not conditioned medium exclusively inhibit the inflammatory response of stimulated T cells: implications for nanomedicine. Theranostics. 2017 Jan 1;7(2):270-284